一次性使用输液器在我国临床上广泛使用, 目前我国输液器生产中多使用环己酮作为部件粘合剂粘接成型, 环已酮是一种化学溶剂, 有强烈的刺激性, 其沸点为155.6℃, 容易残留在产品的粘接处及内腔中。环己酮会在输液过程中进入病人血液, 对人体造成损害, 更甚者可能造成严重的临床不良反应。环己酮属于有毒溶剂, 动物实验中发现环己酮对中枢神经系统有抑制作用, 较长时间接触可引起皮肤刺激造成皮炎, 对眼粘膜有明显刺激和角膜损害[1]。有研究表明体外循环类产品中环己酮的残留物会损害心血管功能[2]。因此分析、控制输液器中环己酮的残留量十分必要。
现行国家标准中未对输液器中环己酮残留量的检测方法和限量进行规定。目前医疗器械中环己酮的测定方法有碱性碘化汞钾显色法[3]、分光光度法[4]、气相色谱法[5,6,7,8,9,10]、气相色谱–质谱联用法[11,12]、光电离-离子迁移谱法[13]、电喷雾萃取电离–三重四极杆质谱法[14]等。以上分析方法中有的只能给出定性指标, 有的操作烦琐、重现性差, 有的仪器价格昂贵、分析成本高, 难以广泛应用于产品质量控制中。顶空气相色谱测定易挥发性有机溶剂具有操作简便、基体干扰小、准确度高、重复性好, 检测结果可靠等优点, 笔者采用气相色谱结合顶空进样方式, 建立了一种具有高选择性、准确度、灵敏度, 可行且适用于一次性使用输液器中环己酮残留量的分析方法, 通过对不同厂家输液器中环己酮残留量的测定, 了解目前在临床中使用的一次性输液器中环己酮残留量的大体状况, 为今后研究、制定该项目的质量标准奠定基础。
1 实验部分
1.1 主要仪器与试剂
气相色谱仪, 配HS40顶空进样器,
公司;
电子天平:AL204–IC型, 瑞士梅特勒–托利多公司;
循环泵蠕动泵:BT00–300T型, 保定兰格恒流泵有限公司;
精密振荡水浴锅:SW23型, 德国JULABO有限公司;
环己酮标准物质:纯度为99.9%, 德国Dr.Ehrenstorfer公司;
乙醇:色谱纯, 上海安谱实验科技股份有限公司;
超纯水系统:Human Power I型, 韩国Human公司;
实验所用样品为一次性使用输液器 (带针) 、一次性使用精密过滤输液器 (带针) ;
实验用水为超纯水。
1.2 仪器工作条件
1.2.1 气相色谱
检测器:FID;色谱柱:Elite–5柱 (30 m×0.32mm, 0.25μm) ;柱温:程序升温, 初始温度为50℃, 保持3 min, 以10℃/min升温至100℃, 保持2min, 再以20℃/min升温至170℃, 保持2 min;检测器温度:250℃;进样口温度:230℃;分流比:5∶1;流量:2 m L/min。
1.2.2 顶空条件
炉温:80℃;取样针温度:90℃;传输线温度:100℃;平衡时间:30 min。
1.3 实验步骤
1.3.1 样品预处理
采用两种方式制备样品: (1) 取一套一次性使用输液器, 以60滴/min的流速模拟临床进行滴注纯水24 h。用试剂瓶收集流出液 (注意瓶口以封口膜密封) 作为检验液, 取2~20 m L顶空瓶中, 密封测定; (2) 循环浸提法将3套灭过菌的输液器和一只300m L硅硼玻璃烧瓶连成封闭循环系统, 将烧瓶置于能使其中的液体温度保持在 (37±1) ℃的加热器上, 加入水250 m L, 以1 L/h的流量使之循环2 h。用一蠕动泵作用在一段尽可能短的硅胶管上, 输液器若配有静脉针, 制备试验液时, 需将静脉针的管路部分切成1 cm长的段, 将其浸入循环系统玻璃烧瓶的循环液中, 与串联的输液器一起制备检验液, 收集全部浸提液并冷却[15]。取2 m L置于20 m L顶空瓶中, 加盖密封测定。按制备样品浸提液的步骤制备空白液, 回路上不装输液器。
1.3.2 标准溶液配制
精密称取环己酮标准物质0.098 7 g, 加入盛有适量水的10 m L容量瓶中, 以0.2 m L乙醇溶解, 用水稀释至10 m L。精密量取该溶液5 m L, 用水稀释至100 m L。再量取该溶液10 m L, 用水稀释至50 m L, 得到质量浓度为98.7μg/m L的环己酮标准使用液。
2 结果与讨论
2.1 平衡时间
平衡时间的长短取决于被测组分分子从样品基质到气相的扩散速度。将样品在80℃分别平衡10, 20, 30, 40 min后进行测定, 色谱峰面积与平衡时间的关系如图1所示。从图1可以看出, 色谱峰面积随着平衡时间的延长而增大, 平衡时间超过30min后, 峰面积基本不再增加, 证明样品达到了气液两相平衡, 故本实验选取平衡时间为30 min。
图1 平衡时间与色谱峰面积的关系曲线
2.2 平衡温度
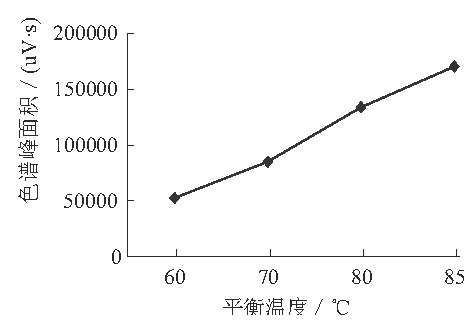
温度对顶空平衡体系的影响较为显著, 顶空温度应根据所选溶剂的特性及待测物质的沸点来选择。以水为溶剂及测定低沸点残留溶剂时, 顶空温度不宜超过85℃。若温度过高, 水蒸气会影响检测器和色谱柱, 并且过高的温度可能导致某些组分分解和氧化。分别将样品在60, 70, 80, 85℃下平衡30min进行测定, 色谱峰面积与平衡温度的关系如图所示2。从图2可以看出, 随着温度的升高, 色谱峰面积逐渐增大, 原因是组分的饱和蒸气压随平衡温度的升高而变大。考虑到平衡温度过高会引起顶空瓶耐压超限和气密性变差等问题, 本实验选择平衡温度为80℃。
图2 平衡温度与色谱峰面积关系
2.3 专属性试验
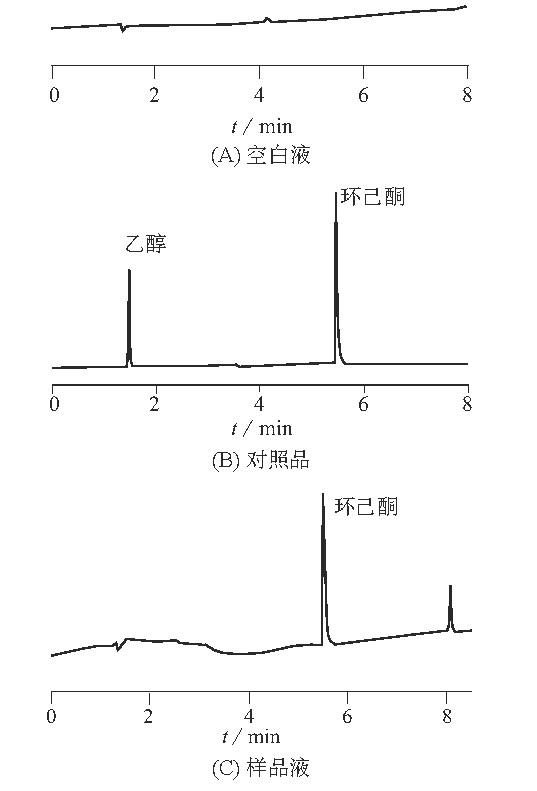
由于很多注射用药的溶剂为水, 所以选择水作为浸提溶剂。只有在均匀的体系中, 才能获得较好的分析精密度和准确度, 因环己酮微溶于水, 根据“相似相溶”的原理, 在配制标准使用液时加入乙醇作为助溶剂。分别精密取空白液 (水) 、环己酮标准溶液、样品溶液, 在1.2仪器工作条件下测定, 色谱图见图3。由图3可知, 水、乙醇对环己酮的测定无干扰, 环己酮的理论塔板数大于6 000, 分离度大于1.5。
2.4 标准工作曲线
分别精密量取环己酮标准使用液0.05, 0.15, 0.50, 1.0, 1.5, 2.0, 3.0, 4.0, 5.0, 6.0, 10.0 m L至10m L容量瓶中, 加水稀释至标线, 得到质量浓度分别为0.494, 1.480, 4.935, 9.870, 14.805, 19.740, 29.610, 39.480, 49.350, 59.220, 98.700μg/m L的环己酮系列标准溶液, 分别取2 m L标准溶液至20 m L顶空瓶中, 加盖密封测定。结果表明, 在0.494~98.700μg/m L范围, 环己酮的质量浓度与色谱峰面积有良好的线性关系, 相关系数r=0.999 9。
图3 空白液、对照品及样品液的气相色谱图
2.5 检出限与定量限
取环己酮标准溶液逐级稀释, 进样测定, 以3倍信噪比测得检出限为0.094μg/m L, 以10倍信噪比测得定量限为0.313μg/m L。
2.6 精密度试验
分别精密量取质量浓度为4.935, 19.740µg/m L的环己酮标准溶液, 平行测定6次, 测定结果见表1。由表1可知, 环己酮色谱峰面积测定结果的相对标准偏差均小于1%, 表明方法的精密度良好。
表1 精密度试验结果 下载原表
2.7 加标回收试验
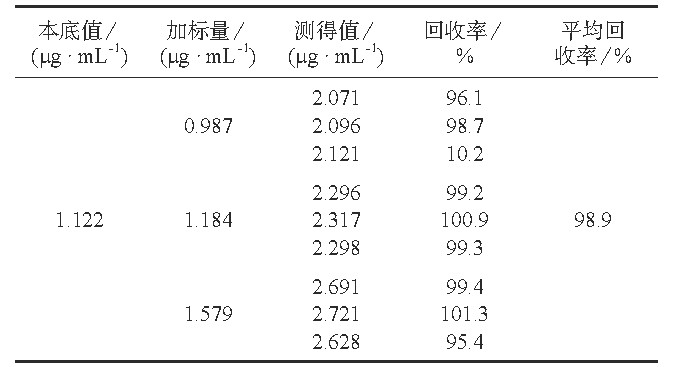
精密量取已测定环己酮含量的样品溶液 (24 h模拟输液) 8 m L 9份, 分别置于10 m L容量瓶中。各精密加入19.740µg/m L环己酮标准溶液0.5, 0.6, 0.8 m L, 每种浓度制备3份样品溶液, 用水稀释至标线。精密量取已测定环己酮含量的样品液 (2 h循环浸提法) 7 m L 9份, 分别置于10 m L容量瓶中。各精密加入98.70µg/m L环己酮标准溶液1.5, 2.0, 2.5 m L, 每种浓度制备3份, 用水稀释至标线。用本法对以上溶液进行测定, 测定结果分别见表2, 表3。由表2, 表3可知, 24 h模拟输液样品液平均回收率为为98.9% (n=9) , 循环浸提样品液平均回收率为99.4% (n=9) , 表明本法测定结果准确、可靠。
表2 24 h模拟输液样品加标回收试验结果 下载原表
表3 循环浸提样品加标回收试验结果 下载原表
2.8 样品液的测定
选取11个省18家生产企业的29批次输液器进行测定, 结果均有环己酮溶出量检出, 且环己酮的残留量存在差异, 这种差异不仅存在于不同企业的产品之间, 也存在于同一企业不同批次产品之间。采用24 h模拟临床输液制备的样品液, 输液器中环己酮最小值为2.0 mg/套, 最大值为10.9 mg/套。采用2 h循环浸提法制备的样品液, 输液器中环己酮最小值为0.30 mg/套, 最大值为4.4 mg/套。
对医疗器械产品进行浸提的目的是利用适宜的浸提方法 (浸提时间、浸提温度、浸提介质、介质体积等) 制备出试验样品, 经化学分析测定溶出物中待测物质的量, 用于对人体健康风险性的评价。理想的浸提方法既要反映产品的实际使用条件, 又要反映试验的目的和预测性。由于通常情况下一次性输液器的使用时间不超过24 h, 循环浸提法既结合了临床使用情况, 又易操作可控, 所以宜选用此法进行样品液的制备。
3 结语
(1) 采用顶空气相色谱法测定输液器中环己酮, 方法操作简单、快速, 测定结果准确、可靠, 适用于一次性使用输液器和输血器中环己酮残留量测定。
(2) 不同厂家的输液器残留量差异很大, 可能与各厂家生产条件, 人工操作、贮存条件、储存时间、外包装透气性能等因素有关。因此有必要在我国输液器国家标准中增加环己酮残留量的限量要求及对应的检测方法, 在规定限量时, 应对不同厂家的产品进行考察, 系统研究, 使累积的数据更具有代表性和科学性, 从而合理地对限量值作出规定, 尽可能避免环己酮在产品中的残留对人体造成损伤。